【第十八改正日本薬局方より】シラザプリル水和物:本品は定量するとき、換算した脱水物に対し、シラザプリル(C22H31N3O5:417.50)98.5~101.0%を含む。
シラザプリル錠:本品は定量するとき、表示量の93.0~107.0%に対応するシラザプリル(C22H31N3O5:417.50)を含む。
【メモ】0.25mg錠も、0.5mg錠も、1mg錠も、後発品のみの医薬品です。
因みに、先発品のインヒベース錠0.25・0.5・1(中外製薬)は経過措置になりました。
| 先発品・準先発品・後発品 | 規格 | 品名 | 画像 | 性状 | 割線の有無 | 直径/長径/垂線/長辺(mm) 厚さ(mm) 重さ(mg) 印字 |
添加物 | 貯法 | 製造販売業者等 | 添付文書PDF | IF PDF |
| 後発品 | 0.25mg1錠 | シラザプリル錠0.25mg「トーワ」 |  |
白色のフィルムコーティング錠 | 直径/長径/垂線/長辺(mm) 5.1 厚さ(mm) 2.4 重さ(mg) 54 印字(企業マークは除く) Tw 033/0.25 |
乳糖水和物、トウモロコシデンプン、ポビドン、クロスカルメロースNa、ショ糖脂肪酸エステル、ヒプロメロース、ヒドロキシプロピルセルロース、タルク、酸化チタン | 室温保存(開封後は湿気に注意) | 東和薬品株式会社 | 添付文書190411 | インタビューフォーム | |
| 後発品 | 0.25mg1錠 | シラザプリル錠0.25mg「サワイ」 | 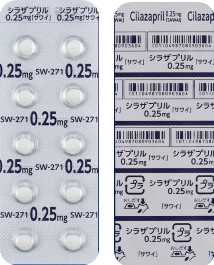 |
白色のフィルムコーティング錠 | 直径/長径/垂線/長辺(mm) 5.1 厚さ(mm) 2.4 重さ(mg) 約54 印字(企業マークは除く) SW 271 /0.25 |
クロスカルメロースNa、酸化チタン、ショ糖脂肪酸エステル、タルク、トウモロコシデンプン、乳糖、ヒドロキシプロピルセルロース、ヒプロメロース、ポビドン | 室温保存、開封後は湿気を避けて保存 | 沢井製薬株式会社 | 添付文書190410 | インタビューフォーム | |
| 後発品 | 0.5mg1錠 | シラザプリル錠0.5mg「トーワ」 | 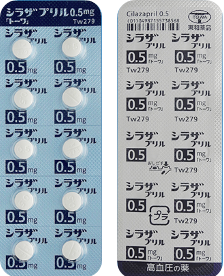 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 5.6 厚さ(mm) 2.5 重さ(mg) 62.8 印字(企業マークは除く) Tw 279/0.5 |
乳糖水和物、トウモロコシデンプン、ポビドン、クロスカルメロースNa、ショ糖脂肪酸エステル、ヒプロメロース、ヒドロキシプロピルセルロース、タルク、酸化チタン | 室温保存(開封後は湿気に注意) | 東和薬品株式会社 | 添付文書190411 | インタビューフォーム |
| 後発品 | 0.5mg1錠 | シラザプリル錠0.5mg「サワイ」 | 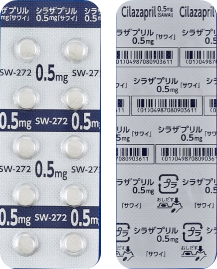 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 5.6 厚さ(mm) 2.5 重さ(mg) 約63 印字(企業マークは除く) SW 272 |
クロスカルメロースNa、酸化チタン、ショ糖脂肪酸エステル、タルク、トウモロコシデンプン、乳糖、ヒドロキシプロピルセルロース、ヒプロメロース、ポビドン | 室温保存、開封後は湿気を避けて保存 | 沢井製薬株式会社 | 添付文書190410 | インタビューフォーム |
| 後発品 | 1mg1錠 | シラザプリル錠1mg「トーワ」 |  |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7.1 厚さ(mm) 3.1 重さ(mg) 125 印字(企業マークは除く) Tw 277 |
乳糖水和物、トウモロコシデンプン、ポビドン、クロスカルメロースNa、ショ糖脂肪酸エステル、ヒプロメロース、ヒドロキシプロピルセルロース、タルク、酸化チタン | 室温保存(開封後は湿気に注意) | 東和薬品株式会社 | 添付文書190411 | インタビューフォーム |
| 後発品 | 1mg1錠 | シラザプリル錠1mg「サワイ」 | 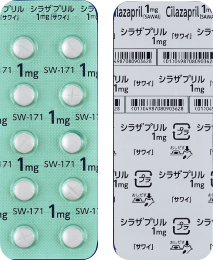 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7.1 厚さ(mm) 3.3 重さ(mg) 約132 印字(企業マークは除く) SW 171 |
カルナウバロウ、結晶セルロース、硬化油、酸化チタン、ショ糖脂肪酸エステル、トウモロコシデンプン、乳糖、ヒドロキシプロピルセルロース、ヒプロメロース | 室温保存、開封後は湿気を避けて保存 | 沢井製薬株式会社 | 添付文書190410 | インタビューフォーム |