【第十八改正日本薬局方より】フロセミド:本品を乾燥したものは定量するとき、フロセミド(C12H11ClN2O5S)98.0~101.0%を含む。
フロセミド錠:本品は定量するとき、表示量の95.0~105.0%に対応するフロセミド(C12H11ClN2O5S:330.74)を含む。
【薬品名の印字】10mg錠と40mg錠において、NIGとSNに、20mg錠において、JGとNIGとSNに、薬品名の印字がある。
【後発品のみ】エルメッドエーザイより、細粒剤の4%細粒あり。
因みに、先発品のラシックス細粒4%(サノフィ)は経過措置になりました。
錠剤
| 先発品・準先発品・後発品 | 規格 | 品名 | 画像 | 性状 | 割線の有無 | 直径/長径/垂線/長辺(mm) 厚さ(mm) 重さ(mg) 印字 |
添加物 | 貯法 | 製造販売業者等 | 添付文書PDF | IF PDF |
| 準先発品 | 10mg1錠 | ラシックス錠10mg |  |
微赤色の裸錠 | 割線入り | 直径/長径/垂線/長辺(mm) 8 厚さ(mm) 2.3 重さ(mg) 0.15g 印字(企業マークは除く) DLT/10 |
結晶セルロース、乳糖水和物、トウモロコシデンプン、ヒドロキシプロピルセルロース、アミノアルキルメタクリレートコポリマーE、ステアリン酸マグネシウム、軽質無水ケイ酸、三二酸化鉄 | 室温保存 | サノフィ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 10mg1錠 | フロセミド錠10mg「NP」 |  |
微赤色の素錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7 厚さ(mm) 3 重さ(mg) 150 印字(企業マークは除く) NP 217/10 |
結晶セルロース、乳糖水和物、トウモロコシデンプン、ヒドロキシプロピルセルロース、アミノアルキルメタクリレートコポリマーE、ステアリン酸マグネシウム、軽質無水ケイ酸、三二酸化鉄 | 室温保存、遮光保存 | ニプロ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 10mg1錠 | フロセミド錠10mg「NIG」 | 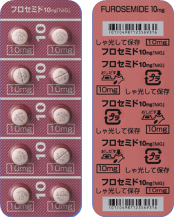 |
微赤色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6.1 厚さ(mm) 3.1 重さ(mg) 95 印字(企業マークは除く) フロセミド TV 10 |
カルナウバロウ、軽質無水ケイ酸、結晶セルロース、酸化チタン、ステアリン酸マグネシウム、トウモロコシデンプン、乳糖水和物、ヒプロメロース、部分アルファー化デンプン、マクロゴール6000、メチルセルロース、三二酸化鉄 | 遮光保存、気密容器保存 | 日医工岐阜工場株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 10mg1錠 | フロセミド錠10mg「SN」 | 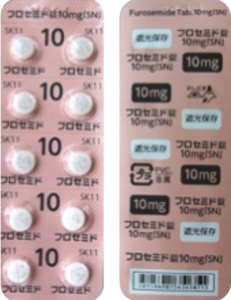 |
微赤色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6.1 厚さ(mm) 3.1 重さ(mg) 95 印字(企業マークは除く) フロセミド 10 SK 11 |
乳糖水和物、トウモロコシデンプン、結晶セルロース、軽質無水ケイ酸、部分アルファー化デンプン、メチルセルロース、ステアリン酸マグネシウム、ヒプロメロース、マクロゴール6000、酸化チタン、三二酸化鉄、カルナウバロウ | 室温保存、遮光保存、気密容器保存 | シオノケミカル株式会社 | 添付文書220623 | インタビューフォーム |
| 準先発品 | 20mg1錠 | ラシックス錠20mg |  |
白色の裸錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6 厚さ(mm) 2 重さ(mg) 0.08g 印字(企業マークは除く) DLF/20 |
乳糖水和物、トウモロコシデンプン、部分アルファー化デンプン、タルク、ステアリン酸マグネシウム、軽質無水ケイ酸 | 室温保存 | サノフィ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 20mg1錠 | フロセミド錠20mg「NP」 |  |
微黄色の素錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7.1 厚さ(mm) 3 重さ(mg) 150 印字(企業マークは除く) NP 212/20 |
結晶セルロース、乳糖水和物、トウモロコシデンプン、ヒドロキシプロピルセルロース、アミノアルキルメタクリレートコポリマーE、ステアリン酸マグネシウム、軽質無水ケイ酸、黄色三二酸化鉄 | 室温保存、遮光保存 | ニプロ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 20mg1錠 | フロセミド錠20mg「JG」 | 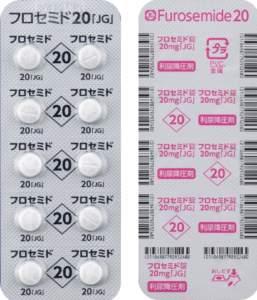 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6.1 厚さ(mm) 3.1 重さ(mg) 97 印字(企業マークは除く) フロセミド 20 JG |
乳糖水和物、トウモロコシデンプン、結晶セルロース、軽質無水ケイ酸、部分アルファー化デンプン、アルファー化デンプン、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール6000、カルナウバロウ | 室温保存、遮光保存、気密容器保存 | 日本ジェネリック株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 20mg1錠 | フロセミド錠20mg「NIG」 | 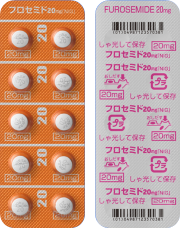 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6.1 厚さ(mm) 3.1 重さ(mg) 97 印字(企業マークは除く) フロセミド TV 20 |
アルファー化デンプン、カルナウバロウ、軽質無水ケイ酸、結晶セルロース、酸化チタン、ステアリン酸マグネシウム、トウモロコシデンプン、乳糖水和物、部分アルファー化デンプン、ヒプロメロース、マクロゴール6000 | 遮光保存、気密容器保存 | 日医工岐阜工場株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 20mg1錠 | フロセミド錠20mg「SN」 | 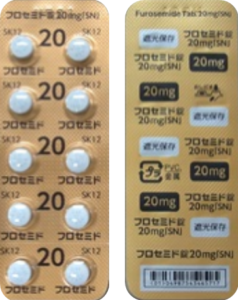 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 6.1 厚さ(mm) 3.1 重さ(mg) 97 印字(企業マークは除く) フロセミド 10 SK 12 |
乳糖水和物、トウモロコシデンプン、結晶セルロース、軽質無水ケイ酸、部分アルファー化デンプン、アルファー化デンプン、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール6000、カルナウバロウ | 室温保存、遮光保存、気密容器保存 | シオノケミカル株式会社 | 添付文書220623 | インタビューフォーム |
| 準先発品 | 40mg1錠 | ラシックス錠40mg | 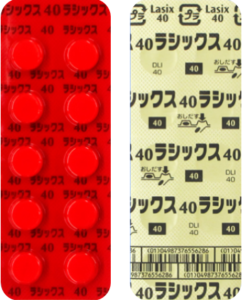 |
白色の裸錠 | 割線入り | 直径/長径/垂線/長辺(mm) 8 厚さ(mm) 2.3 重さ(mg) 0.16g 印字(企業マークは除く) DLI/40 |
乳糖水和物、トウモロコシデンプン、部分アルファー化デンプン、タルク、ステアリン酸マグネシウム、軽質無水ケイ酸 | 室温保存 | サノフィ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 40mg1錠 | フロセミド錠40mg「NP」 | 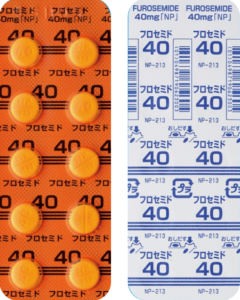 |
白色の素錠 | 割線入り | 直径/長径/垂線/長辺(mm) 8 厚さ(mm) 2.2 重さ(mg) 150 印字(企業マークは除く) NP 213/40 |
トウモロコシデンプン、乳糖水和物、結晶セルロース、カルメロースカルシウム、ステアリン酸マグネシウム、タルク | 室温保存、遮光保存 | ニプロ株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 40mg1錠 | フロセミド錠40mg「トーワ」 | 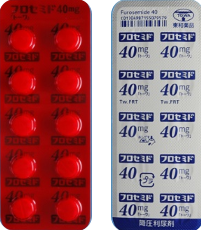 |
白色の素錠 | 割線入り | 直径/長径/垂線/長辺(mm) 8 厚さ(mm) 3 重さ(mg) 200 印字(企業マークは除く) Tw FRT |
乳糖水和物、アルファー化デンプン、トウモロコシデンプン、低置換度ヒドロキシプロピルセルロース、ステアリン酸MG | 室温保存、遮光保存 | 東和薬品株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 40mg1錠 | フロセミド錠40mg「JG」 |  |
白色の素錠 | 割線入り | 直径/長径/垂線/長辺(mm) 8 厚さ(mm) 2.5 重さ(mg) 160 印字(企業マークは除く) JG 40 |
乳糖水和物、トウモロコシデンプン、D-マンニトール、低置換度ヒドロキシプロピルセルロース、ヒドロキシプロピルセルロース、ヒプロメロースフタル酸エステル、ステアリン酸マグネシウム | 室温保存、遮光保存、気密容器保存 | 日本ジェネリック株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 40mg1錠 | フロセミド錠40mg「NIG」 | 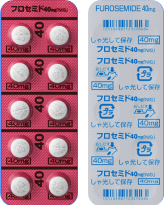 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7.6 厚さ(mm) 3.8 重さ(mg) 191 印字(企業マークは除く) フロセミド TV 40 |
アルファー化デンプン、カルナウバロウ、軽質無水ケイ酸、結晶セルロース、酸化チタン、ステアリン酸マグネシウム、トウモロコシデンプン、乳糖水和物、部分アルファー化デンプン、ヒプロメロース、マクロゴール6000 |
遮光保存、気密容器保存 |
日医工岐阜工場株式会社 | 添付文書220623 | インタビューフォーム |
| 後発品 | 40mg1錠 | フロセミド錠40mg「SN」 | 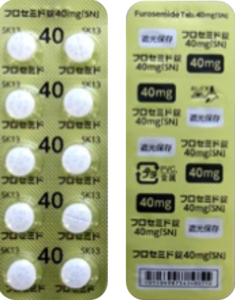 |
白色のフィルムコーティング錠 | 割線入り | 直径/長径/垂線/長辺(mm) 7.6 厚さ(mm) 3.8 重さ(mg) 191 印字(企業マークは除く) フロセミド 10 SK 13 |
乳糖水和物、トウモロコシデンプン、結晶セルロース、軽質無水ケイ酸、部分アルファー化デンプン、アルファー化デンプン、ステアリン酸マグネシウム、ヒプロメロース、酸化チタン、マクロゴール6000、カルナウバロウ | 室温保存、遮光保存、気密容器保存 | シオノケミカル株式会社 | 添付文書220623 | インタビューフォーム |
細粒剤
| 先発品・準先発品・後発品 | 規格 | 品名 | 性状 | 添加物 | 貯法 | 製造販売業者等 | 添付文書PDF | IF PDF | 後発品のみ |
| 後発品 | 4%1g | フロセミド細粒4%「EMEC」 | 白色の細粒 | カルメロースカルシウム、タルク、乳糖水和物、ヒドロキシプロピルセルロース、D‐マンニトール | 室温保存、開封後光を遮り湿気を避けて保存 | エルメッドエーザイ株式会社 | 添付文書220623 | インタビューフォーム |  |